 |
TUM School of Natural Sciences |
 |
Chemische Wirkung des Stromes (Elektrolyse)
Kurzbeschreibung
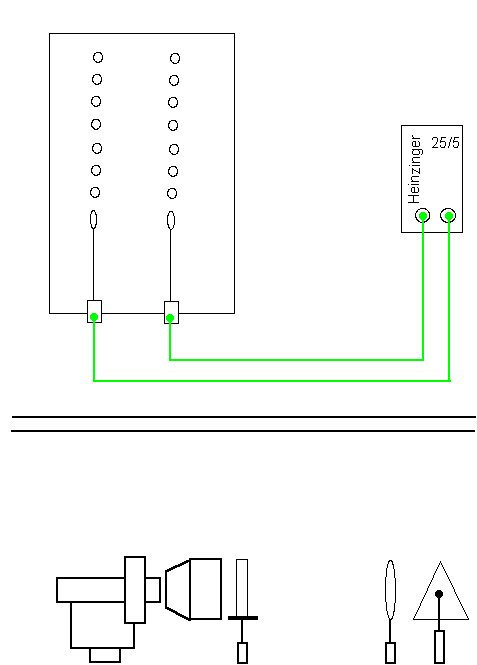
Eine Küvette mit zwei eingeschmolzenen Elektroden wird auf dem Pohltisch aufgebaut und optisch abgebildet. Die Elektroden schließt man an eine Gleichspannungsquelle an. Die Küvette wird dann mit Wasser gefüllt, dem man einige Tropfen verdünnte Schwefelsäure (20%) zusetzt. Bei Stromdurchgang sieht man von den Elektroden Bläschen aufsteigen.
Betriebsanleitungen:Lampen, Elektrogeräte, Schwefelsäure
Physikalische Erklärung
Für die Elektrolyse von Wasser lautet das Gesamt-Reaktionsschema dieser Redoxreaktion:2H2O → Elektrolyse → 2H2 + O2
Sie besteht aus zwei Teilreaktionen, die jeweils an der Kathode und Anode stattfinden.
Die Teilreaktionen sind
an der Kathode: 2 H3O+ + 2 e− → H2 + 2 H2O
an der Anode: 6 H2O → O2 + 4 H3O+ + 4 e−
Haftungsausschluss Datenschutz
Copyright © 2011 Josef Kressierer